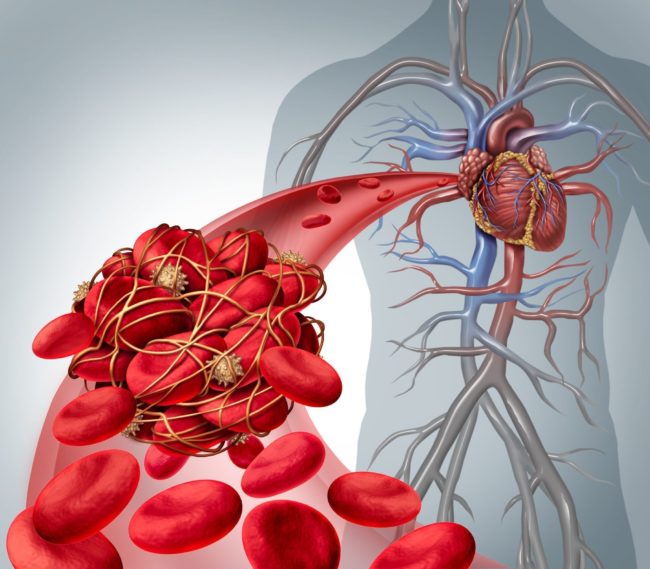
Le trombofilie ereditarie sono difetti genetici della coagulazione. Si definisce trombofilia un quadro clinico predisponente alla formazione di coaguli e di conseguenza di episodi trombotici. Si ha un evento trombotico, venoso o arterioso, quando il sangue (anche in piccole quantità) coagula all’interno di un vaso sanguigno, aderisce alla sua parete e lo ostruisce in maniera parziale o completa, impedendo il flusso del sangue. Il coagulo prende il nome di trombo.
Il Laboratorio Analisi Biomedicals si avvale di attrezzature all’avanguardia e esegue in sede test molecolari basati su Real Time PCR, gold standard per test genetici per screening di difetti genetici predispongono alla trombofilia ereditaria.
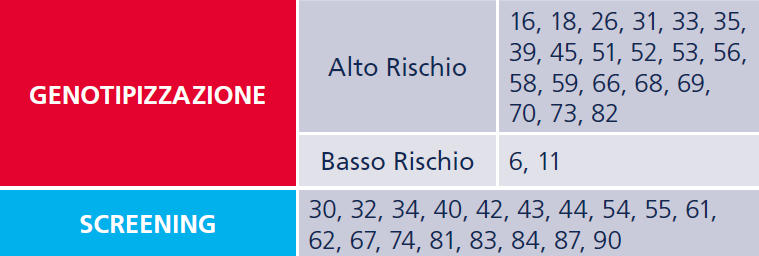
BASI GENETICHE DELLA TROMBOFILIA EREDITARIA
Le varianti geniche oggi note responsabili di difetti genetici correlati a trombosi sono nella maggior parte dei casi delle mutazioni puntiformi ad un singolo nucleotide (SNP) che presentano una tale frequenza nella popolazione da essere considerate delle varianti polimorfiche. I geni in considerazione sono quelli relativi al FATTORE V, al FATTORE II della coagulazione (protrombina), il gene MTHFR (Metilen-tetraidrofolatoreduttasi) , il gene PAI-1,PLASMINOGEN ACTIVATOR INHIBITOR 1. Nella popolazione la maggior parte delle varianti genetiche si presenta in forma eterozigote, cioè i soggetti sono portatori di una mutazione in una delle due copie del gene; essi hanno una possibilità su due di trasmettere la variante genetica alla progenie, indipendentemente dal sesso. Gli individui in cui sono alterate entrambe le copie del gene sono definiti omozigoti. L’analisi del DNA permette di identificare gli individui portatori di una specifica mutazione, sia in eterozigosi che omozigosi.
FATTORE V
Il fattore V attivato è un cofattore essenziale per l’attivazione della protrombina (fattore II) a trombina. Il suo effetto pro-coagulante è normalmente inibito dalla Proteina C attivata. Del fattore V sono note 2 varianti geniche diffuse nella popolazione europea correlate alla trombofilia ereditaria.
-
-
-
-
- mutazione R506Q o di Leiden: presente nel 3-5% della popolazione generale. Tale variante ha una frequenza genica dell’1,4 – 4,2% in Europa con una frequenza di portatori in eterozigosi in Italia pari al 2-3%; l’omozigosità per tale mutazione ha un’ incidenza di 1:5000. I soggetti eterozigoti hanno un rischio 8 volte superiore di sviluppare una trombosi venosa, mentre gli omozigoti hanno un rischio pari ad 80 volte. Tale evento trombotico è favorito in presenza di altre condizioni predisponenti quali la gravidanza, l’assunzione di contraccettivi orali (rischio aumentato di 30 volte negli eterozigoti e di alcune centinaia negli omozigoti), gli interventi chirurgici. In gravidanza una condizione genetica di eterozigosi per il Fattore Leiden è considerata predisponente all’aborto spontaneo, alla eclampsia, ai difetti placentari, alla Sindrome HELLP (emolisi, elevazione enzimi epatici, pastrinopenia. Tali manifestazioni sarebbero legate a trombosi delle arterie spirali uterine con conseguente inadeguata perfusione placentare. I soggetti portatori di mutazione del fattore V di Leiden dovrebbero pertanto sottoporsi a profilassi anticoagulativa in corso di gravidanza o in funzione di interventi chirurgici ed evitare l’assunzione di contraccettivi orali.
- mutazione H1299R (HR2): Diversi studi mirati alla valutazione di una sua associazione con il fenotipo APC-resistance e con fenomeni trombotici hanno riconosciuto tale mutazione come un fattore di rischio protrombotico confermabile da un significativo abbassamento dei valori di APC-ratio in vitro e da un aumentato rischio protrombotico in quei soggetti che ereditavano in trans l’aplotipo e la mutazione Leiden. Inoltre soggetti con l’aplotipo HR2 hanno un aumento relativo della isoforma più trombogenica e glicosilata del FV (FV1)
FATTORE II – Protrombina
Il Fattore II della coagulazione o Protrombina, per azione del Fattore V viene trasformata in trombina che svolge un ruolo fondamentale nella formazione del coagulo.
La mutazione G20210A è presente nel 2-4% della popolazione. Provoca aumentati livelli del Fattore II (protrombina) funzionale nel plasma e conseguente aumentato rischio di trombosi, specie di tipo venosa. La frequenza genica della variante è bassa (1.0 – 1.5%) con una percentuale di eterozigoti del 2-3%. L’evento trombotico è favorito anche in presenza di altre condizioni quali l’assunzione di contraccettivi orali (da 15 a 30 volte). I soggetti omozigoti per la mutazione sono invece rari.
METILEN-TETRAIDROFOLATO REDUTTASI (MTHFR)
il gene MTHFR codifica per un enzima chiamato Metilen-tetraidrofolato reduttasi che catalizza la rimetilazione dell’omocisteina in metionina. L’analisi del DNA consente di identificare due varianti geniche del gene MTHFR correlate a trombofilia ereditaria. la mutazione C677T nel gene MTHFR che determina, specialmente negli omozigoti, una riduzione dell’attività enzimatica del 50% che, quindi, è meno efficiente, nel convertire l’omocisteina in metionina; questo comporta un aumento dei livelli di omocisteina nel sangue (omocisteinemia) e nelle urine (omocisteinuria), specie dopo carico orale di metionina. La frequenza genica in Europa della mutazione è del 3-3,7% che comporta una condizione di eterozigosi in circa il 42-46% della popolazione e di omozigosi pari al 12-13%.
Recentemente, una seconda mutazione del gene MTHFR (A1298C) è stata associata ad una ridotta attività enzimatica (circa il 60% singolarmente; circa il 40% se presente in associazione alla mutazione C677T). Questa mutazione, in pazienti portatori della mutazione C677T, determina un’aumento dei livelli ematici di omocisteina.
Livelli aumentati di omocisteina nel sangue sono oggi considerati fattore di rischio per malattia vascolare, (trombosi arteriosa) forse attraverso un meccanismo mediato dai gruppi sulfidrilici sulla parete endoteliale dei vasi. Inoltre in condizioni di carenza alimentare di acido folico la variante termolabile della MTHFR porta a livelli molto bassi l’acido folico nel plasma ed è pertanto un fattore di rischio per i difetti del tubo neurale nelle donne in gravidanza.
PLASMINOGEN ACTIVATOR INHIBITOR 1 (PAI-1): mutazione 1-BP DEL/INS, 4G/5G
Il PAI-1(Inibitore dell’attivatore del Plasminogeno) è il maggiore inibitore del sistema fibrinolitico, ed è prodotto da piastrine, cellule endoteliali e muscolari della parete vasale.
La presenza dell’allele 4G, nella maggior parte dei casi in eterozigoti 4G/5G, è associato a livelli sierici di PAI-1 più elevati rispetto a pazienti con polimorfismo 5G/5G, poiché aumenta l’attività trascrizionale del rispettivo gene. Elevate concentrazioni plasmatiche di PAI-1 sono associate ad un rischio aumentato per trombosi sia arteriose che venose in particolar modo in soggetti ipertesi e/o fumatori
A CHI E’ RIVOLTO IL TEST
Lo studio delle varianti geniche correlate a trombofilia ereditaria è indicato in:
-
-
-
-
- Soggetti con precedenti episodi, o familiarità, di tromboembolismo venoso o trombosi arteriosa;
- Donne che intendono assumere contraccettivi orali, con precedenti episodi di trombosi in gravidanza e/o poliabortività, con precedente figlio con DTN ( difetto tubo neurale);
- Soggetti sottoposti a terapie farmacologiche a rischio trombotico;
- Gestanti con IUGR, tromboflebite o trombosi placentare;
- Soggetti diabetici, ipertesi e cardiopatici, con elevati livelli sierici di omocisteina e/o colesterolo
In tali situazioni la conoscenza della predisposizione genetica alla trombosi può fornire al medico elementi utili per una adeguata terapia preventiva.
MODALITA’ DI ACCESSO
Il test effettuato nel nostro laboratorio comprende l’analisi delle 6 mutazioni illustrate ed è condotto su campione ottenuto da prelievo venoso. I nostri orari per i prelievi sono i seguenti: dal lunedì al venerdì dalle 7:30 alle 10:00, il sabato dalle 8:00 alle 10:00. Il test non richiede prenotazione né richiesta medica e il risultato è refertato entro 7 giorni